| 語言 : |
|
| 百科社區 |百科問答 |提交問題 |詞彙知識 |上傳知識 |
甲烷 |
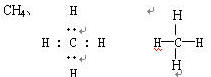 |
|
閃點(℃):-188 引燃溫度(℃):538 分子直徑0.414nm 標準狀況下密度為0.717g/L,極難溶於水[1]CAS號:74-82-8[1] 化學性質 取代反應 把一個大試管分成五等分,或用一支有刻度的量氣管,用排飽和食鹽水法先收集1/5體積的甲烷,再收集4/5體積的氯氣,把它固定在鐵架台的鐵夾上,並讓管口浸沒在食鹽水里。然後讓裝置受漫射光照射。在陽光好的日子,約半小時後可以看到試管內氯氣的黃綠色逐漸變淡,管壁上出現油狀物,這是甲烷和氯氣反應的所生成的一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳(或四氯甲烷)和少量的乙烷的混合物。試管中液面上升,食鹽水中白色晶體析出,這是反應中生成的氯化氫溶於水的緣故。因為氯化氫極易溶於水,溶於水後增加了水中氯離子的濃度,使氯化鈉晶體析出。 [2]用大拇指按住試管管口,提出液面,管口向上,向試管中滴入紫色石蕊試液或鋅粒,可驗證它是稀鹽酸。如果在陰暗的天氣需1到2小時才能觀察到反應的結果。 CH4 Cl2→(光照)CH3Cl(氣體) HCl 此時,無明顯反應現象。 CH3Cl Cl2→(光照)CH2Cl2(油狀物) HCl 此時,現象為試管壁上出現油狀小液滴。 CH2Cl2 Cl2→(光照)CHCl3(油狀物) HCl 此時,現象為試管內有白霧出現。 CHCl3 Cl2→(光照)CCl4(油狀物) HCl 此時,現象為黃綠色氣體逐漸變無色。 最後生成的HCl最多 注:甲烷可與溴產生類似反應。甲烷與氟的反應十分猛烈,如果先用稀有氣體稀釋兩者才在特定的儀器內進行反應,也可得出類似反應。甲烷與碘不會直接產生反應,可以用溴化碘等代替進行碘化。 [3] 氧化反應 點燃純淨的甲烷,在火焰的上方罩一個乾燥的燒杯,很快就可以看到有水蒸氣在燒杯壁上凝結。倒轉燒杯,加入少量澄清石灰水,振盪,石灰水變渾濁。說明甲烷燃燒生成水和二氧化碳。把甲烷氣體收集在高玻璃筒內,直立在桌上,移去玻璃片,迅速把放有燃燒著的蠟燭的燃燒匙伸入筒內,燭火立即熄滅,但瓶口有甲烷在燃燒,發出淡藍色的火焰。這說明甲烷可以在空氣里安靜地燃燒,但不助燃。用大試管以排水法先從氧氣貯氣瓶裡輸入氧氣2/3 體積,然後再通入1/3 體積的甲烷。用橡皮塞塞好,取出水面。將試管顛倒數次,使氣體充分混和。用布把試管外麵包好,使試管口稍微下傾,拔去塞子,迅速用燃著的小木條在試管口引火,即有尖銳的爆鳴聲發生。這個實驗雖然簡單,但也容易失敗。把玻璃導管口放出的甲烷點燃,把它放入貯滿氯氣的瓶中,甲烷將繼續燃燒,發出紅黃色的火焰,同時看到有黑煙和白霧。黑煙是炭黑,白霧是氯化氫氣體和水蒸氣形成的鹽酸霧滴。 加熱分解 在隔絕空氣並加熱至1000℃的條件下,甲烷分解生成炭黑和氫氣 CH4=高溫=C 2H2 氫氣是合成氨及汽油等工業的原料;炭黑是橡膠工業的原料 氯化 甲烷在紫外光或熱(250∼400℃)作用下,與氯反應得各種氯代烷。 如果控制氯的用量,用大量甲烷,主要得到氯甲烷;如用大量氯氣,主要得到四氯化碳。工業上通過精餾,使混合物一一分開。以上幾個氯化產物,均是重要的溶劑與試劑。 甲烷氯化反應的事實是: ①在室溫暗處不發生反應; ②髙於250℃發生反應; ③在室溫有光作用下能發生反應; ④用光引發反應,吸收一個光子就能產生幾千個氯甲烷分子; ⑤如有氧或有一些能捕捉自由基的雜質存在,反應有一個誘導期,誘導期時間長短與存在這些雜質多少有關。根據上述事實的特點可以判斷,甲烷的氯化是一個自由基型的取代反應。 [4] 鹵化 |
| 用戶 評論 |
|
還沒有評論 |